- אודותינו
- מחקר
- סטודנטים והוראה
- סמינרים וארועים
- בעלי תפקידים
- הזמנת חדרים ומיכשור
- English
דף הבית » פרופ' בת שבע כרם פיתחה תרופה חדשה לטיפול בחולי Cystic fibrosis
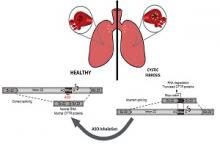
סיסטיק פיברוזיס (CF) הינה מחלה גנטית מסכנת ומקצרת חיים, הנגרמת על ידי מוטציות שונות בגן ה- Cystic Fibrosis Transmembrane Conductance Regulator (CFTR) . גן זה מקודד לתעלת כלוריד(Cl-) , הממוקמת על פני תאי אפיתל לאורך מערכת הנשימה, בדרכי העיכול ובבלוטות האקסוקריניות. פעילות לקויה של תעלת ה- CFTR מובילה לשינוי במאזן האלקטרוליטים והנוזלים על פני האפיתל ולהצטברות של ריר סמיך (ראו סימון ירוק בחלק העליון של התמונה). הריר הסמיך אשר מצטבר לאורך עץ סימפונות הריאה מהווה מצע להתרבות חיידקים, פוגע ביכולת חילוף הגזים, ומוביל למחלת ריאות כרונית אשר מהווה את הגורם העיקרי לתחלואה ולתמותה.
המטרה שהצבנו במחקר הנוכחי היתה פיתוח טיפול חדש לחולי CF הנושאים את המוטציה 3849+10kb C-to-T . מוטציה זו גורמת לשחבור לא תקין של מולקולות ה-RNA המתורגמות מגן ה- CFTR. (בתהליך השחבור נחתכים מספר מקטעי RNA מתוך מולקולת ה־RNA הראשונית, המשועתקת מן ה-DNA, ונוצר ה־RNA הבוגר.)
המוטציה הנ"ל גורמת להכללה של רצף שגוי במולקולות ה-RNA הבוגר, אשר מובילה לפירוק מולקולות ה-RNA או לחילופין ליצירת חלבון קצר ולא פעיל (ראו חלק ימני תחתון של התמונה). מוטציה זו היא השביעית בשכיחותה בארה"ב והשמינית בשכיחותה באירופה, ונישאת על ידי כ- 1600 חולי CF בעולם. המוטציה שכיחה באוכלוסיות מסויימות כגון יהודים אשכנזים וחולי CF בסלובניה, פולין ואיטליה.
היות והטיפולים התרופתיים הזמינים כיום לחולי CF נותנים רק מענה מוגבל לחולים הנושאים מוטציות שחבור, יש צורך באסטרטגיות נוספות לפיתוח תרופות אשר יתנו מענה לחולים הנושאים מוטציה זו.
במחקר הנוכחי, שבוצע בשיתוף עם חברתSpliSense , התמקדנו בגישה ייחודית המתבססת על מולקולות המכונות אנטיסנס אוליגונוקליאוטידים (antisense oligonucleotides), אשר ביכולתן להיקשר לרצפים ספציפיים לאורך מולקולות ה-RNA ולהשפיע על תהליך השחבור. סריקה של כ- 30 מולקולות אנטיסנס אוליגונוקליאוטידים במודל תאי הובילה לזיהוי של מספר מולקולות, אשר הצליחו לתקן באופן יעיל את דפוס שחבור ה-RNA ולמנוע את הכללת הרצף השגוי.
בשלב זה נבדקה יעילות המולקולות הנבחרות בתאי אפיתל, אשר מקורם ממערכת הנשימה של חולי CF הנושאים לפחות עותק אחד של המוטציה 3849+10kb C-to-T. תרביות אלה מהוות מערכת מודל משמעותית בשלבים הפרה-קליניים של המחקר. מצאנו כי למולקולות הנבחרות היתה יכולת משמעותית לתקן את דגם שחבור ה-RNA וכן את פעילות תעלת ה- CFTR. מולקולות האנטיסנס אוליגונוקליאוטידים הצליחו לחדור ביעילות לתאי האפיתל באמצעות ספיגה חופשית ללא שימוש בנשא.
בהמשך ניסינו לבדוק את ההשפעה של מולקולות הכוללות שינויים כימיים שונים במטרה לשפר את יעילותן. לאחר בחינה של יעילות המולקולות הנבחרות במערכות תאיות שונות שמקורן מחולי CF שונים, זיהינו מולקולה מובילה אשר הראתה יעילות גבוהה בתיקון דגם השחבור ושיקום מלא של התפקוד התקין של התעלה.
רמות פעילות תעלת ה- CFTR לאחר הטיפול במולקולה המובילה צפויות להעניק יתרון קליני משמעותי לחולים ולשפר את איכות חייהם. התוצאות שהושגו במחקר הנוכחי מהוות את הבסיס לפיתוח קליני של המולקולה המובילה על ידי חברת SpliSense . התרופה החדשה תינתן באינהלציה לחולי CF הנושאים את המוטציה.